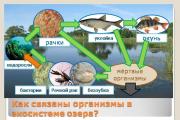
Особенности кругооборота воды и некоторых веществ в биосфере. Кислород в природе (49,4% в Земной коре) Круговорот кислорода в природе схема и описание
Химия, 8 класс Дата__________
Урок №___
Тема урока: Свойства и применение кислорода. Круговорот кислорода в природе
Цель урока: изучить физические и химические свойства кислорода, дать общее понятие об оксидах, реакциях горения; рассмотреть
практическую значимость и применение; доказать, что кислород - один из важнейших элементов на Земле.
З адачи урока:
Образовательные :
Расширить представления обучающихся о кислороде.
Познакомить со свойствами и применением кислорода.
Совершенствовать умения составлять уравнения химических реакций.
Воспитательные :
Формировать умения работать в парах у каждого обучающегося, считаться с мнением соседа и отстаивать свою точку зрения корректно, выполняя упражнения.
Воспитывать бережное отношение к своему здоровью, окружающей природе, учить понимать прекрасное, ценить произведения искусства.
Развивающие :
Способствовать продолжению развития устойчивого интереса к химической науке и практике.
Совершенствовать навыки самостоятельной работы, развивать умения наблюдать, формулировать высказывания.
Способствовать развитию исследовательских навыков, соблюдая правила техники безопасности.
Совершенствовать умения обобщать и делать выводы.
Планируемые результаты:
личностные: готовность и способность учащихся к саморазвитию, самоопределению; ответственное отношение к учению; способность ставить цели и строить жизненные планы; формирование коммуникативной культуры, ценности здорового и безопасного образа жизни;
метапредметные: уметь ставить цель и планировать пути её достижения, выбирая более рациональные способы решения данной проблемы; учиться корректировать свои действия в связи с изменением создавшейся ситуации; уметь создавать, применять и преобразовывать знаки и символы, модели и схемы для решения учебных и познавательных задач; уметь осознанно использовать речевые средства в соответствии с задачей коммуникации для выражения своих мыслей и потребностей; уметь организовывать совместную работу со сверстниками в парах; уметь находить информацию в различных источниках; владеть навыками самоконтроля, самооценки;
предметные:
знать : основные химические понятия «катализаторы», «оксиды», «реакции горения», «реакции окисления»; физические и химические свойства кислорода; области применения кислорода.
уметь: отличить кислород от других газов; составлять уравнения реакций горения веществ в кислороде; записывать химические формулы оксидов и давать им названия; объяснять, как происходит круговорот кислорода в природе .
Тип урока: урок формирования умений и навыков.
Форма работы: фронтальная, групповая, работа в парах, игровая.
Методы обучения: словесный, частично-поисковый, наглядный, демонстрационный, интерактивный.
Приемы обучения : постановка проблемных вопросов.
Оборудование: компьютер, проектор, презентация «Свойства и применение кислорода. Круговорот кислорода в природе», пробирка с
газоотводной трубкой, колба, стеклянная пластина, пинцет, ложка для сжигания веществ, штатив, спиртовка, универсальная
индикаторная бумага, химический стакан.
Реактив ы: красный фосфор, вода.
Литература:
Для учителя:
Горковенко М. Ю. Поурочные разработки по химии 8 класс к учебникам О. С. Габриеляна, Л. С. Гузея, Г. Е. Рудзитиса. - М: «ВАКО», 2004;
Радецкий А. М., Горшкова В. П. Дидактический материал: химия 8-9 классы - М: Просвещение, 1997.
Для ученика:
Химия: неорганическая химия: учебник для 8 класса общеобразовательных учреждений/ Г. Е. Рудзитис, Ф. Г. Фельдман. - М: «Просвещение», 2014 г.
Интернет-ресурсы:
http://www.e-osnova.ru/
ХОД УРОКА
І. Организационный момент. (1 мин.) (Слайд №1)
Учитель: Добрый день! Прошу всех садиться. Я поздравляю вас еще с одним чудесным днем. И мы с вами продолжаем творить волшебство на уроках химии.
ІІ. Актуализация знаний. (7 мин.).
Фронтальный опрос «А ну-ка, химики» . (Слайд №2)
Учитель: Сегодня на уроке мы изучим свойства и применение кислорода. Круговорот кислорода в природе. Но перед тем как
приступить к изучению новой темы, вам следует ответить на следующие вопросы: 2 обучающихся получают задание на карточках и
Выполняют его у доски:
На какой диаграмме распределение массовых долей элементов отвечает
количественному составу (NH 4 ) 3 PO 4 ? Ответ: 4.
Фронтальный опрос
Химический знак кислорода? Ответ: О
Относительная атомная масса кислорода? Ответ: 16.
Химическая формула кислорода? Ответ: О2.
Относительная молекулярная масса кислорода? Ответ: 32.
В соединениях кислород обычно какой валентности? Ответ: II.
Расскажите о нахождении кислорода в природе. Ответ: Кислород - самый распространенный химический элемент в земной коре. Кислород - самый распространенный на Земле элемент, на его долю приходится около 49% массы твердой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода - 85,5% (по массе), в атмосфере содержание свободного кислорода составляет 21% по объёму и 23% по массе. Более 1500 соединений земной коры в своем составе содержат кислород. Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет 20,9%, по массовой доле - около 65 %.
Перечислите способы получения кислорода в лаборатории? Ответ:
В лаборатории кислород получают следующими
способами:
1) Разложение перманганата калия. 2KMnO4 = K2MnO4+MnO2+O2
2) Разложение перекиси водорода. 2H2O2 = 2H2O + O2
3) Разложение бертолетовой соли. 2KClO3 = 2KCl + 3O2
8. Перечислите способы получения кислорода в промышленности. Ответ: В промышленности кислород получают:
1) Электролиз воды. 2H2O = 2H2 + O2
2) Из воздуха. ВОЗДУХ давление, -183˚C=O2 (голубая жидкость).
В настоящее время в промышленности кислород получают из воздуха. В лабораториях небольшие количества кислорода можно получать нагреванием перманганата калия (марганцовка) KMnO4. Кислород мало растворим в воде и тяжелее воздуха, поэтому его можно получать двумя способами:
9. Установите соответствие между способом получения кислорода и уравнением химической реакцией. Работа в парах. (Слайд №3)
|
Способы получения кислорода |
Уравнения химических реакций |
|
А. Разложение перманганата калия. Б. Разложение перекиси водорода. В. Разложение бертолетовой соли. Г. Электролиз воды. Д. Из воздуха. |
1) 2KClO 3 = 2KCl + 3O 2 2) 2H 2 O 2 = 2H 2 O + O 2 3) ВОЗДУХ = O 2 4) 2KMn O 4 = K 2 Mn O 4 + Mn O 2 + O 2 5) 2H 2 O = 2H 2 + O 2 |
Ответ: А-4; Б-2; В-1; Г-5; Д-3.
10. Что называют катализаторами? Где эти вещества применяются? Ответ: Вещества, которые ускоряют химические реакции,
но сами при этом не расходуются, называют катализаторами. Катализаторы широко применяют в химической промышленности. С
их помощью удается повысить производительность химических процессов, снизить себестоимость выпускаемой продукции и более
полно использовать сырье.
ІІІ. Изучение нового материала. (12 мин.) (Слайд №4)
Учитель: Физические свойства. Кислород - бесцветный газ, без вкуса и запаха, относительно малорастворим в воде (в 100 объемах
Воды при температуре 20 ºС растворяется 3,1 объема кислорода). Кислород немного тяжелее воздуха: 1л кислорода при нормальных
условиях весит 1,43 г, а 1л воздуха - 1,29г. (Нормальные условия - сокращенно: н.у. - температура 0ºС и давление 760 мм.рт.ст., или
1 атм. ≈ 0,1 МПа). При давлении 760 мм.рт.ст. и температуре -183ºС кислород сжижается, а при снижении температуры до -218,8ºС
затвердевает.
(Слайд №5) Химические свойства. Кислород при нагревании энергично реагирует со многими веществами, при этом выделяются
Теплота и свет. Такие реакции называют реакциями горения. Если опустить в сосуд с кислородом O 2 тлеющий уголек, то он
Раскаляется добела и сгорает, образуя оксид углерода(IV ) С O 2 . Чтобы определить, какое образовалось вещество, в сосуд наливают
Известковую воду - раствор гидроксида кальция Са(ОН) 2 . Она мутнеет, так как при этом образуется нерастворимый карбонат
Кальция СаС O 3 :
CO 2 + Ca(OH) 2 = CaCO 3 ↓ + H 2 O
(Слайд №6) Сера горит в O 2 ярким синим пламенем с образованием газа с резким запахом - оксида серы(IV )
S + O 2 = SO 2
(Слайд №7) Демонстрационный опыт «Горение фосфора в кислороде»
Техника безопасности (провести инструктаж!) Опыт следует проводить под тягой. Следует соблюдать правила обращения с
Нагревательными приборами. Не допускать попадания горящего фосфора на рабочую поверхность стола. Не вдыхать выделяющийся
Дым фосфорного ангидрида.
Фосфор Р сгорает в O 2 ярким пламенем с образованием белого дыма, состоящего из твердых частиц оксида фосфора(V).
4P + 5O 2 = 2P 2 O 5
(Слайд №8) В кислороде горят и такие вещества, которые обычно считают негорючими, например железо. Если к тонкой стальной
Проволоке прикрепить спичку, зажечь ее и опустить в сосуд с кислородом, то от спички загорится и железо. Горение железа
Происходит с треском и разбрасыванием ярких раскаленных искр - расплавленных капель железной окалины Fe3O4. В этом
Соединении два атома железа трехвалентны и один двухвалентен. Поэтому реакцию горения железа в кислороде можно выразить
Следующим уравнением:
3 Fe + 2 O 2 = FeO * Fe 2 O 3 или Fe 3 O 4
(Слайд №9) Взаимодействие вещества с кислородом относится к реакциям окисления .
(Слайд №10) Горение - это химическая реакция, при которой происходит окисление веществ с выделением теплоты и света.
В большинстве случаев при взаимодействии веществ с кислородом образуются оксиды. (Слайд №11) Оксиды - это сложные
Вещества, которые состоят из двух элементов, одним из которых является кислород.
(Слайд №12) Известны химические элементы, которые непосредственно с кислородом не соединяются. К ним относятся золото Au и
Некоторые другие. Оксиды этих элементов получают косвенным путем.
(Слайд №13) Применение кислорода. Основано на его химических свойствах. В больших количествах кислород используют для
Ускорения химических реакций в разных отраслях химической промышленности и в металлургии. Например, при выплавке чугуна
Для повышения производительности доменных печей в них подают воздух, обогащенный кислородом.
(Слайд №14) При сжигании смеси ацетилена или водорода с кислородом в специальных горелках температура пламени достигает
3000 º С. Такое пламя используется для сварки металлов. Если берут кислород в избытке, то пламенем можно резать металл.
(Слайд №15) Жидкий кислород применяют в ракетных двигателях.
(Слайд №16) В медицине кислород служит для облегчения затрудненного дыхания. В этом случае кислородом заполняют
Специальные подушки. Кислородные маски необходимы в высотных полетах, в космосе и при работе под водой.
(Слайд №17) Кислород расходуется в громадных количествах на многие химические реакции, например на сжигание топлива.
(Слайд №18) Из сказанного видно, что очень много кислорода расходуется на разнообразную деятельность человека, тратится на
Процессы дыхания человека, животных, растений, а также на процессы гниения. Человек при дыхании в течение 1 мин в среднем
Употребляет 0,5 дм ³ кислорода, в течении суток - 720 дм ³ , а в год - 262,8 м ³ кислорода, что все жители земного шара (5 миллиардов)
В течение года для дыхания используют 1578 миллиардов кубических метров кислорода. Если такой объем кислорода при нормальном
Давлении поместить в железнодорожные цистерны, то поезд был бы протяженностью более 300 млн км, что равняется расстоянию до
Солнца и обратно.
(Слайд №19) Но все же общая масса кислорода в воздухе заметно не изменяется. Это объясняется процессом фотосинтеза,
Происходящим в зеленых растениях на свету. В результате этого процесса выделяется кислород.
С фотосинтезом вы уже знакомились в курсе ботаники. Упрощенно процесс фотосинтеза изображают так:
6CO 2 + 6H 2 O = C 6 H 12 O 6 + 6O 2 .
Так в природе происходит непрерывный круговорот кислорода.
(Слайд №20) В целях сохранения кислорода в воздухе вокруг городов и крупных промышленных центров создаются зоны зеленых
Насаждений. Специальная служба систематически контролирует содержание кислорода в воздухе. При необходимости применяют
Меры по устранению загрязнения воздуха.
(Слайд №21) Физкультминутка. (1 мин.)
Руки кверху поднимаем,
А потом их отпускаем.
А потом их развернем
И к себе скорей прижмем.
А потом быстрей, быстрей
Хлопай, хлопай веселей.
IV. Закрепление знаний. (6 мин.)
(Слайд №22) Задание №1. «Правда или ложь? Если знаешь - разберешь»
Для кислорода верны следующие утверждения:
а) Кислород – бесцветный газ, без вкуса и запаха .
б) Кислород немного легче воздуха.
в) В кислороде горят и такие вещества, которые обычно считают негорючими, например железо.
г) Известны химические элементы, которые непосредственно с кислородом соединяются. К ним относятся золото Au и некоторые другие.
д) Применение кислорода основано на его физических свойствах.
е) Непрерывный круговорот кислорода непосредственно связан с таким процессом, как фотосинтез.
Ответ: а; в; е.
(Слайд №23) Задание №2. «Скорая помощь»
Вставьте пропущенные вещества в уравнениях реакций:
а) …….. + Ca(OH) 2 = CaCO 3 ↓ + H 2 O
б) S + ……. = SO 2
в) ….. + 2 O 2 = FeO * Fe 2 O 3 или Fe 3 O 4
Ответ: а)CO 2 б)O 2 в) 3 Fe
(Слайд №24) Задание №3. «Мозговой штурм»
Расставьте коэффициенты в уравнениях реакций.
а) CO 2 + H 2 O = C 6 H 12 O 6 + O 2
б) P + O 2 = P 2 O 5
(Слайд №25) Задание №4. «Ассоциации»
С каким применением кислорода ассоциируется данное изображение?
(Слайд №26) 1) в металлургии;
(Слайд №27) 2) в авиации для двигателей;
(Слайд №28) 3) в авиации для дыхания;
(Слайд №29) 4) для резки металлов;
(Слайд №30) 5) для сварки металлов;
(Слайд №31) 6) на взрывных работах;
(Слайд №32) 7) в медицине.
(Слайд №33) V. Домашнее задание. (1 мин.)
§20,21; №6-9 (с.60). Решите задачи 1-2 (с.60).
Творческое задание: подготовить сообщение №10 с. 60 «Что делается в вашей местности для поддержания определенного содержания
Кислорода в воздухе? В чем может заключаться ваше участие в этой деятельности?»
(Слайд №33) VI. Рефлексия. (1 мин.)
Учитель:
С егодня я узнал...
было трудно…
я понял, что…
я научился…
я смог…
было интересно узнать, что…
меня удивило…
мне захотелось…
VII. Подведение итогов урока. (1 мин.)
(Слайд №34)
В чём горят дрова и газ,
Фосфор, водород, алмаз?
Дышит чем любой из нас
Каждый миг и каждый час?
Без чего мертва природа?
Правильно, без….
Обучающиеся:
кислорода
Учитель: Правильно. Спасибо за урок! До свидания! (Слайд №35)
Круговорот кислорода на планете Земля - один из основных процессов, которому обязаны своим существованием все формы жизни. Каковы особенности и главные составляющие этого масштабного действа? Именно на этот вопрос мы попробуем найти ответ.
Характеристика кислорода как элемента
Для того чтобы понять суть глобального процесса, рассмотрим его основную составляющую. Первое, на что обратим внимание, - характеристика кислорода как главного элемента круговорота. Он существует в нескольких видах: собственно оксигениум (или оксиджен) - легкий неметалл таблицы Менделеева, который обозначают латинской буквой O; невидимый безвкусный и бесцветный газ, образованный двумя молекулами O 2 , именуемый дикислород. Этот газ считают самым сильным и распространенным окислителем. Можно выделить и еще одну форму - озон, который представляет собой соединение уже трех молекул O. Кислород - вторая главная составляющая атмосферы нашей планеты, которая, как мы помним, почти на 80% состоит из азота. Немногим менее 20% приходится на долю кислорода.
Главные «потребители» оксигениума

Круговорот кислорода в биосфере Земли - сложный и постоянный процесс, который поддерживает и сохраняет возможность жизнедеятельности животных, растений и человека. В сложном взаимодействии происходит постоянное возобновление запасов этого бесценного газа. Человек и плоды его труда в этом процессе являются главными потребителями. Люди и животные в естественном процессе дыхания поглощают кислород, выдыхая, как всем нам известно, углекислый газ. Промышленные и ресурсодобывающие предприятия, автомобильный транспорт также выделяют в атмосферу огромное количество вредных веществ и примесей, сжигая тонны кислорода и уменьшая процент его в окружающей среде.
Немного о фотосинтезе
Восстановление жизненно важного элемента происходит благодаря такому процессу, как фотосинтез. Преобразование углекислого газа в кислород - заслуга флоры нашей планеты. Именно растения обладают этой удивительной способностью - ежедневно восполнять этот ценный газ, потребленный человеком и представителями животного мира. В чем суть фотосинтеза? Если говорить простым языком, то он является ничем иным, как поглощением из окружающей среды углекислого газа с последующим выделением в

нее кислорода. Наземные растения получают его из атмосферы и земли через корни и листья, а водоросли используют газ, растворенный в воде. Именно благодаря такой особенности жизнедеятельности земной флоры количество кислорода на планете возобновляется в объеме, необходимом для продолжения существования жизни.
Схема круговорота
Если описывать круговорот кислорода схематично, то он будет выглядеть следующим образом: выделение элемента происходит из растений на воде и земле. Недавно учеными было доказано, что небольшая часть этого газа появляется и в самой атмосфере как следствие разложения водного пара под воздействием солнечных лучей. Поглощают его люди, животные, промышленные предприятия. Круговорот кислорода можно сравнить с работой легких человека. Именно он позволяет нашей планете дышать - к сожалению, с каждым годом делать это Земле все сложнее.
Кислород - самый распространенный элемент земной коры. В свободном состоянии он находится в атмосферном воздухе, в связанном виде входит в состав воды, минералов, горных пород и всех веществ, из которых построены организмы растений и животных. Массовая доля кислорода в земной коре составляет около 47%.
Кислород - бесцветный газ, не имеющий запаха. Он немного тяжелее воздуха. Кислород играет исключительно важную роль в природе. При участии кислорода совершается один из важнейших жизненных процессов - дыхание . Важное значение имеет и другой процесс, в котором участвует кислород - тление и гниение погибших животных и растений; при этом сложные органические вещества превращаются в более простые (в конечном результате в CO 2 , воду и азот) , а последние вновь вступают в общий круговорот веществ в природе.
Кислород - наиболее активный газ. В пределах биосферы происходит быстрый обмен кислорода среды с живыми организмами или их остатками после гибели.
В составе земной атмосферы кислород занимает второе место после азота. Господствующей формой нахождения кислорода в атмосфере является молекула О 2 . Круговорот кислорода в биосфере весьма сложен, поскольку он вступает во множество химических соединений минерального и органического миров.
Главным образом круговорот кислорода происходит между атмосферой и живыми организмами. В основном свободный кислород (О 2) поступает в атмосферу в результате фотосинтеза зеленых растений, а потребляется в процессе дыхания животными, растениями и микроорганизмами, и при минерализации органических остатков (гниения различных веществ). Незначительное количество кислорода образуется из воды и озона под воздействием ультрафиолетовой радиации.
В истории биосферы Земли наступило такое время, когда количество свободного кислорода достигло определенного уровня и оказалось сбалансированным таким образом, что количество выделяемого кислорода стало равным количеству поглощаемого кислорода.
Большое количество кислорода расходуется на окислительные процессы в земной коре, при извержении вулканов и т.д.
Основная доля кислорода продуцируется растениями суши - почти 3/4, остальная часть - фотосинтезирующими организмами Мирового океана. Скорость круговорота - около 2 тыс. лет.
Установившиеся в биосфере объемы потоков кислорода и кислородосодержащих соединений в современных условиях нарушаются техногенными миграциями. Промышленные, бытовые и сельскохозяйственные отходы, сброшенные в природные воды (реки, озера, моря, океаны), связывают растворенный в воде кислород, что также нарушает объемы кислородных потоков в биосфере. Загрязнение почв, сведение лесов уменьшает обмен кислородом и диоксидом углерода между атмосферой и сушей. Однако запасы кислорода на планете неисчерпаемы. Он входит в состав кристаллических решеток минералов и высвобождается из них при помощи живого вещества. Поэтому для поддержания установившихся объемов кислородных потоков в биосфере необходимо сохранение живого вещества как главной геохимической силы.
Установлено, что на промышленные и бытовые нужды ежегодно расходуется 23% кислорода, который образуется в процессе фотосинтеза, и эта цифра постоянно возрастает.
Кислород атмосферы накоплен в результате деятельности зеленых растений. Потребовалось около 2,5–3 млрд.лет для создания современного состава атмосферы, содержащей 21% кислорода.
Весь свободный кислород в атмосфере оценивается в 1,6×10 9 т. Это его количество потребляется на дыхание живыми организмами за 2 тыс.лет, что и составляет время полного круговорота кислорода в биосфере.
Круговорот кислорода в биосфере (Клауд, Джибор, 1972)
У верхней границы тропосферы под влиянием космических излучений из кислорода образуется озон. Следовательно, озоновый экран, предохраняющий жизнь от смертоносных излучений, также результат деятельности живого вещества, то есть жизнь сама защищает себя от смерти. Этот факт подтверждает гипотезу Ген, по которой глобальные процессы, определяющие пределы жизни, регулируются только биологическими процессами самой биосферы.
Все в мире состоит из химических элементов. Они же поддерживают жизнь на Земле. Одну из важнейших ролей в этом деле играет кислород. С ним связано множество интересных фактов, а круговорот кислорода в природе удивителен. Хотите знать больше? Читайте далее.
Итак, что интересного связано с кислородом:
1. Производят не только растения.
Многим со школьной скамьи известно, что оксиген образуется в результате фотосинтеза растений. Да, именно преобразование углекислого газа растительностью - основной источник кислорода на Земле. Однако он не единственный.
Часть газа образуется в верхних слоях атмосферы под действием солнечных лучей. Нагреваясь, молекулы воды распадаются на составные части, образуя водород и кислород.
Кроме того, около половины всего свободного кислорода на планете производит фитопланктон. Углекислый газ, который они потребляют, попадает в атмосферу в результате дыхания животных и людей, а также во время окисления, то есть сгорания.
Просто круговорот кислорода в биосфере можно описать так:
- Под действием солнечного тепла вода из мирового океана испаряется. Ее часть, попадая в верхний слой атмосферы, распадается на H2 и O2.
- Кислород, в свою очередь, перерабатывается живыми существами, которые выделяют углекислый газ. Также угарный газ попадает в атмосферу в результате сгорания материи.
- В процессе фотосинтеза углекислый газ преобразуется снова в кислород.
Примечание: также оксиген выделяется из известняка путем выветривания породы.
2. Кислород использовали алхимики.
Об этом элементе было известно еще в VIII веке. Первые упоминания встречаются в рукописях китайского ученого-алхимика Мао Хоа. Конечно, тогда кислород имел совсем другое название, да и о его свойствах мало что было известно.
Легендарный художник, инженер, биолог и химик Леонардо да Винчи изучал кислород, но даже не догадывался, что кислород - это отдельный элемент.
Однако официальное открытие кислорода произошло в 1774 году. Статус первооткрывателя достался Джозефу Пристли, которому удалось выделить кислород из оксида ртути. Ученый долго не мог понять, почему во время нагревания материала свеча, которая служила источником света, горела намного ярче. Впоследствии Пристли назвал это явление «Второй воздух». Но, как часто бывает в научном мире, здесь не обошлось без скандала.
Позже стало известно, что шведский естествоиспытатель Карл Шееле смог выделить кислород из оксида азота в 1771 году. Данные об эксперименте он записал в свою книгу, которую, к несчастью, издали только через шесть лет.
3. Кислород нужен везде.
Применение кислорода не ограничивается простым дыханием. Его широко используют как окислитель в металлургии. Без него было бы невозможно производство качественной стали. Также газ используется в ацетиленовых и водородных горелках для резки и сварки металла.
Кислород обеспечивает работу тепловых электростанций. Двигателя внутреннего сгорания никогда бы не было, так как наличие оксигена - главное условие детонации топливной смеси.
Космонавты, военные летчики и аквалангисты используют для дыхания баллоны, наполненные кислородом в связке с гелием или другими инертными газами. Таким образом, кислород способствует исследованию океанов и космоса.
4. Кислород - источник красоты и здоровья.
Кислород широко применяется в медицине и при изготовлении косметических средств. С его помощью спасают от удушья, гипоксии, приступов астмы и людей с болезнями сердечно-сосудистой системы.
Безалкогольные коктейли с высоким содержанием оксигена полезны для беременных женщин. Кислородный напиток способствует нормальному развитию плода. Также подобные составы улучшают психоэмоциональное состояние человека, и придают бодрости.
Оксиген добавляют в косметические кремы и маски. Эти средства улучшают состояние кожи, омолаживают и придают эластичности.
5. Три триллиона тонн кислорода в год.
Примерно столько кислорода вырабатывает вся зеленая растительность Земли. Крупнейшими природными фабриками этого газа считаются леса Амазонки и сибирская тайга. Эти места называют «легкими планеты».
Примечание: одно большое дерево вырабатывает достаточно кислорода, чтобы обеспечить двух человек - примерно 125 кг газа в год.
6. Концентрация кислорода снижается.
Несмотря на кажущийся внушительным объем выработки, содержание кислорода в атмосфере составляет в лучшем случае 21%. В больших городах это значение опускается до 18%. К слову, всего несколько миллионов лет назад этот показатель был в два раза выше.
Причина снижения концентрации кислорода в увеличении количества автомобильного транспорта, производственных выбросов и неконтролируемой вырубке лесов.
7. Что будет, если кислород исчезнет на одну секунду?
Если это случится, мир, который мы знаем, перестанет существовать. Нет, растения не завянут, а животные не задохнутся. Все будет значительно хуже. Оксиген входит в состав практически всего и всех.
Бетонные здания тут же рухнут, моря и океаны испарятся, живые существа высохнут и превратятся в пыль. Как дополнение к апокалиптической картине представьте, что земная кора разверзлась, а небо стало черным как ночь.
Увеличение количества оксигена в 10 раз также не сулит ничего хорошего, хотя последствия не будут столь драматичными. Этот сценарий чреват массовым вымиранием из-за гипервентиляции легких. Однако скорее всего жизнь не исчезнет, а возродится в иной форме.
8. В земле кислорода больше, чем в воздухе.
Мало кто знает, но основной запас кислорода сосредоточен не в атмосфере. Свободного кислорода на планете всего 0,36%, при этом около 99,5% газа входит в состав горных пород, силикатов, мантии и земной коры.
9. Эра гигантов стала возможной благодаря кислороду.
До начала господства динозавров, 300 миллионов лет назад, концентрация кислорода была в десятки раз больше. Ученые считают, что во многом благодаря этому на Земле долгое время правили гиганты.
В те далекие времена на планете можно было встретить сороконожку длинной 2,5 метра. Среди ящеров самым большим был Дредноут. Его длина достигала 26–30 м, а вес - 60 тонн.
Относительно недавно благодаря оксигену по планете ходил шестиметровый ленивец. А как насчет двухметрового кабана, который питался преимущественно мясом?! Некоторые млекопитающие, например индрикотерий, чей рост достигал 8 м, а вес 15 тонн, не уступали в размерах динозаврам.
Первобытные люди успели поохотиться на мамонта, который почти в два раза превосходил по размерам современного слона. В последний ледниковый период бок о бок с человеком разумным обитали медведи под три метра в холке и двухметровые олени.
10. Ком в горле и пересыхающие глаза.
При сильном стрессе у человека инстинктивно учащается дыхание. Нередко увеличивается и объем вдыхаемого кислорода за раз. Из-за этого голосовая щель расширяется, вызывая ощущение кома в горле.
Примечание: нередко ком в горле - это симптом серьезных заболеваний, поэтому, если со временем подобное ощущение не проходит, обратитесь к врачу.
Те, кто поднимался высоко в горы, сталкивался с синдромом сухого глаза. Это неприятное ощущение объясняется низким содержанием кислорода на большой высоте. Дело в том, что роговица не содержит сосудов, а питательные вещества и оксиген доставляются к ней через слезные железы наружным способом.
Круговорот кислорода - поразительный процесс. Представить сложно, как на нашей планете все взаимосвязано и насколько хрупка эта связь. Поэтому мы, как разумные существа, должны взять на себя ответственность за сохранение баланса в природе.
>>
Круговорот Оксигена в природе. Применение кислорода
В этом параграфе речь идет:
Совокупность процессов, происходящих в природе, при которых атомы или ионы элемента в результате реакций переходят от одних веществ к другим, называют круговоротом элемента.
Круговорот Оксигена.
Если главным веществом в круговороте Оксигена выбрать кислород, то можно выделить такие звенья круговорота (схема 8):
Расходование, или связывание, кислорода (процессы дыхания, сгорания топлива и горючего, окисление различных веществ в природе, в технологических процессах);
Взаимопревращение оксигенсодержащих соединений;
Схема 8. Круговорот Оксигена (основные звенья)
Образование кислорода (процесс фотосинтеза, разложение воды в верхних слоях атмосферы).
Неизменность содержания кислорода в атмосфере свидетельствует о том, что процессы связывания и выделения кислорода компенсируют друг друга.
Оксиген способствует круговороту других элементов, поскольку образует с ними многочисленные соединения.

Схема 9. Применение кислорода
Кислород используют в различных отраслях , причем в больших количествах (схема 9). В металлургии он ускоряет процесс выплавки стали и улучшает ее качество. Этот газ необходим в производстве многих химических соединений, используется в специальных устройствах для резки и сварки металлов (водороднокислородные, ацетиленово-кислородные горелки).
Баллоны, наполненные кислородом (рис. 66) или его смесью с инертным газом
гелием, используют космонавты, военные летчики, пожарники, водолазы.

Рис. 66. Баллон с кислородом
Кислородные подушки применяют при некоторых заболеваниях для облегчения дыхания. С помощью сжиженного кислорода создают необходимые условия для сгорания горючего в космических ракетах.
Широко используется и кислород, входящий в состав воздуха. При его участии сгорает топливо на теплоэлектростанциях, горючее в двигателях автомобилей, обжигают металлические руды на заводах цветной металлургии.
Это интересно
Отравление угарным газом CO происходит потому, что он реагирует с гемоглобином, и поступление кислорода в организм прекращается.
Во время сжигания топлива и горючего образуется и попадает в воздух значительное количество угарного (CO) и сернистого (SO 2) газов. Эти вещества негативно влияют на растения, вызывают и обостряют болезни у людей. Поэтому в каждой стране работу промышленности, энергетики, транспорта организуют так, чтобы уменьшить количество вредных выбросов в атмосферу. Охрана воздуха от техногенных загрязнений является важным государственным делом.
Биологическая роль кислорода.
Кислород необходим живым существам для дыхания. Попадая через легкие в организм, этот газ соединяется с гемоглобином (компонент крови) и поступает во все органы и ткани. При участии кислорода происходят различные реакции. Некоторые из них сопровождаются выделением теплоты; благодаря этому поддерживается постоянная температура тела.
Выводы
В природе атомы Оксигена в результате химических реакций постоянно переходят от одних веществ к другим; происходит круговорот этого элемента.
Кислород широко используется в промышленности, технике, медицине, а в составе воздуха - в теплоэнергетике, автотранспорте, других областях.
Кислород необходим живым существам. Попадая в организм во время дыхания, он принимает участие во многих химических реакциях. Кислород также является продуктом фотосинтеза.
?
154. Как вы понимаете термин «круговорот»?
155. Напишите два-три уравнения реакций, при которых происходит связывание кислорода.
156. Какие меры должно предпринимать человечество для сохранения баланса кислорода в атмосфере?
157. Известно, что вместо определенного объема кислорода, потребляемого при дыхании, в воздух поступает такой же объем углекислого газа. Определите объемную долю кислорода в выдыхаемом воздухе, если объемная доля углекислого газа в нем составляет 5 %.
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. - К.: ВЦ «Академія», 2008. - 136 с.: іл.
Содержание урока конспект урока и опорный каркас презентация урока интерактивные технологии акселеративные методы обучения Практика тесты, тестирование онлайн задачи и упражнения домашние задания практикумы и тренинги вопросы для дискуссий в классе Иллюстрации видео- и аудиоматериалы фотографии, картинки графики, таблицы, схемы комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты Дополнения рефераты шпаргалки фишки для любознательных статьи (МАН) литература основная и дополнительная словарь терминов Совершенствование учебников и уроков исправление ошибок в учебнике замена устаревших знаний новыми Только для учителей календарные планы учебные программы методические рекомендации